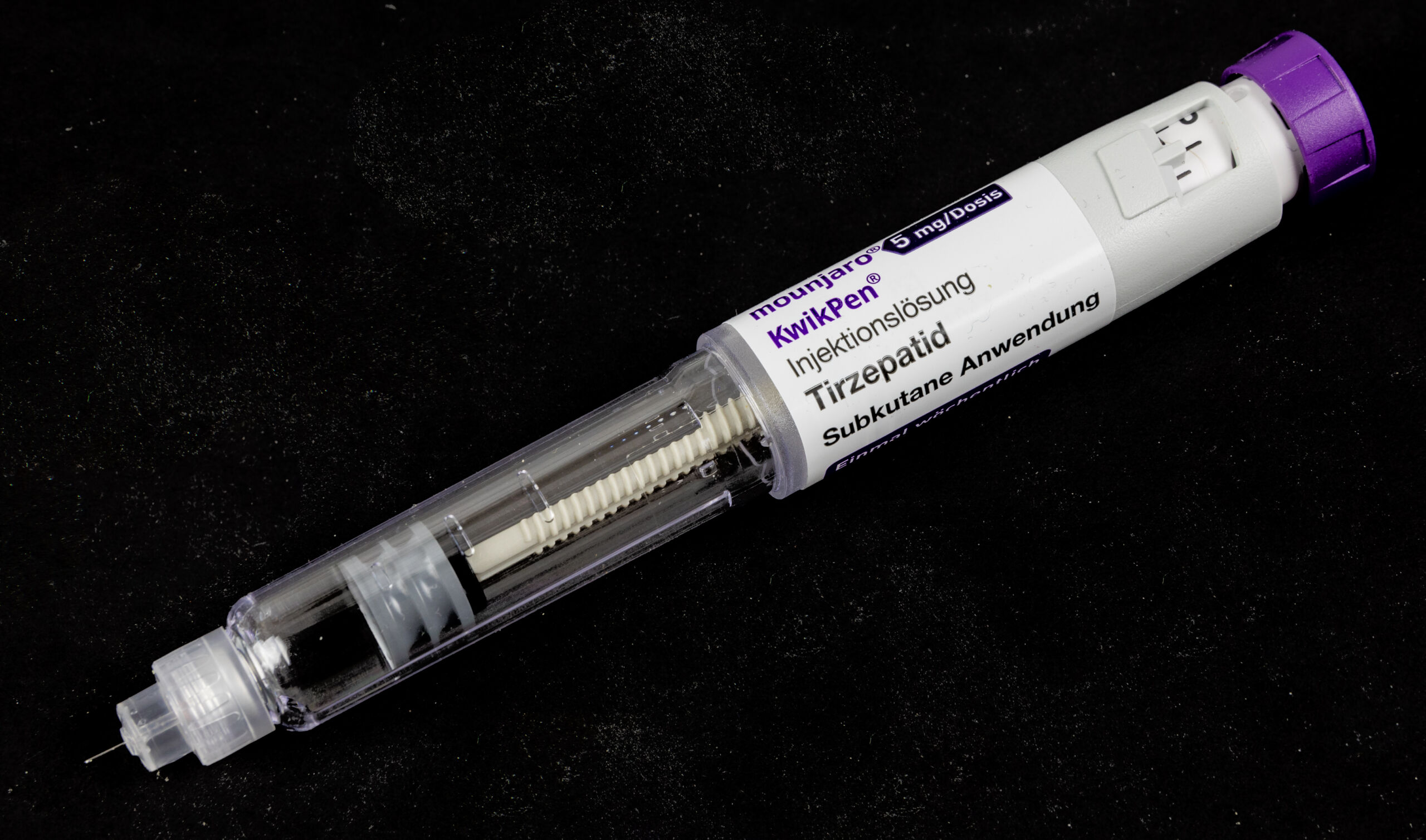
A Agência Nacional de Vigilância Sanitária aprovou o registro do Mounjaro Multidose, nova apresentação do medicamento à base de tirzepatida indicado para o tratamento do diabetes tipo 2. A decisão foi publicada no Diário Oficial da União desta quarta-feira, dia 18, por meio da Resolução-RE nº 1.041, da Gerência-Geral de Medicamentos da Anvisa. O registro foi concedido à farmacêutica Eli Lilly do Brasil com validade de 24 meses.
A principal diferença em relação ao modelo já disponível no mercado está no formato da caneta aplicadora. Enquanto a versão tradicional é de uso único, o Mounjaro Multidose permite que o paciente utilize o mesmo dispositivo para mais de uma aplicação, o que tende a tornar o tratamento mais conveniente no dia a dia. O registro aprovado contempla seis concentrações diferentes do produto, todas em solução injetável de aplicação subcutânea: 4,17 mg/mL, 8,33 mg/mL, 12,5 mg/mL, 16,7 mg/mL, 20,8 mg/mL e 25 mg/mL.
A tirzepatida, princípio ativo do Mounjaro, atua sobre hormônios relacionados ao controle da glicose e do apetite, mecanismo que contribui tanto para o manejo do diabetes tipo 2 quanto para a redução de peso corporal. O medicamento pertence à mesma classe das chamadas canetas emagrecedoras, cujo uso tem crescido de forma expressiva no Brasil nos últimos anos.
Com o registro aprovado pela Anvisa, a nova versão multidose está autorizada a ser comercializada no país. A chegada efetiva às farmácias, no entanto, ainda depende de etapas complementares, como a definição de preço e a estratégia de lançamento a ser adotada pela fabricante.
